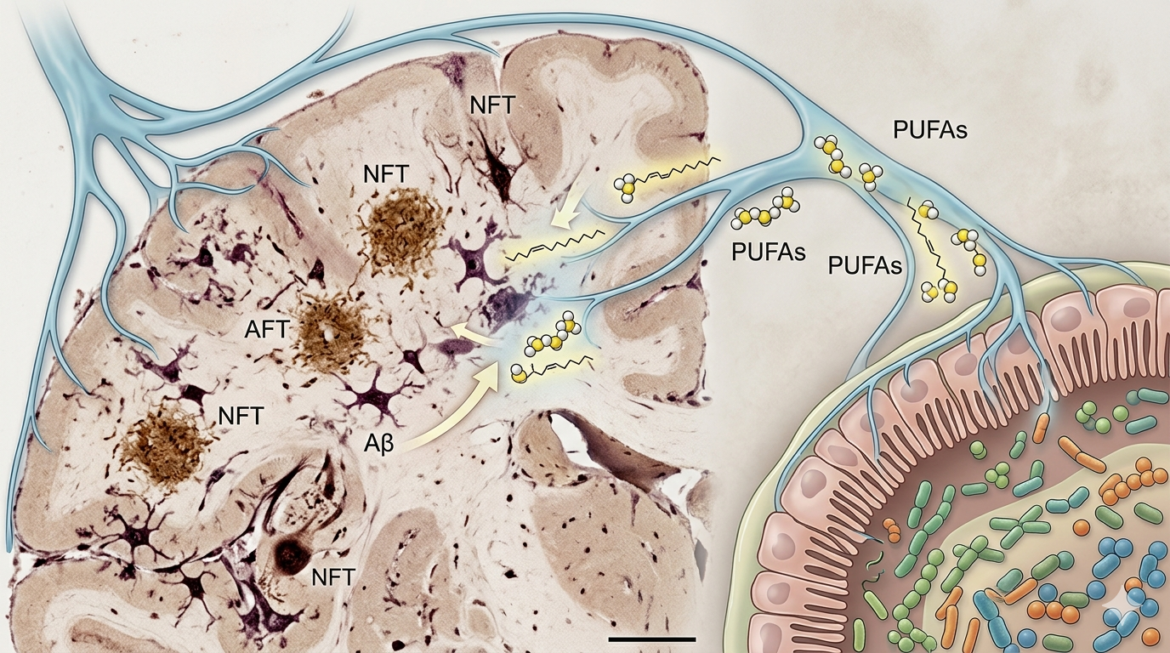
A Doença de Alzheimer (DA) tem sido historicamente abordada sob uma perspectiva neurocêntrica, focada no acúmulo cerebral de proteína beta-amiloide (Aβ) e tau. Contudo, evidências científicas disruptivas, como as apresentadas no estudo de Chen et al. (2022), revelam que a microbiota intestinal exerce um controle regulatório fundamental sobre as patologias da DA e os transtornos cognitivos. Através de uma comunicação complexa via eixo microbiota-intestino-cérebro, microrganismos específicos e seus metabólitos modulam cascatas inflamatórias que determinam a progressão da neurodegeneração, apontando a disbiose intestinal não apenas como um biomarcador, mas como um driver etiológico da doença.
Investigações detalhadas em modelos de camundongos 3xTg-AD demonstraram que a ausência de microbiota (animais germ-free) ou a sua supressão via antibióticos reduz drasticamente a ativação microglial e a formação de placas amiloides. O estudo identifica que a microbiota de indivíduos com DA é caracterizada por uma redução na abundância de bactérias benéficas, como as do gênero Bacteroides (especificamente B. fragilis, B. intestinalis e B. xylanisolvens). Essa alteração na composição microbiana resulta em um desequilíbrio metabólico sistêmico, com destaque para a via de sinalização dos ácidos graxos poli-insaturados (PUFAs). A diminuição de Bacteroides está associada a uma regulação negativa da via de sinalização C/EBPβ/AEP no cérebro, que é crucial para o processamento proteolítico da APP (proteína precursora amiloide) e da tau.
Um dos mecanismos moleculares centrais elucidados pela pesquisa é a modulação da enzima asparagina endopeptidase (AEP), também conhecida como legumaína. Em estados de disbiose, a ativação do fator de transcrição C/EBPβ no cérebro induz a expressão da AEP, que cliva a proteína tau e a APP, gerando fragmentos neurotóxicos que aceleram a formação de agregados insolúveis. O estudo demonstra que o tratamento com B. fragilis ou seus metabólitos é capaz de inibir essa via inflamatória, reduzindo os níveis de mediadores pró-inflamatórios como o leucotrieno B4 (LTB4). O LTB4, derivado do metabolismo do ácido araquidônico, atua como um potente quimioatraente e ativador microglial, exacerbando a neuroinflamação e o dano sináptico.
Além disso, a pesquisa destaca que a transferência de microbiota de pacientes com DA para camundongos saudáveis é suficiente para induzir déficits cognitivos e patologias semelhantes à Alzheimer, confirmando o caráter transmissível desses traços fenotípicos via componentes microbianos. Por outro lado, a restauração da microbiota com cepas específicas de Bacteroides promoveu uma melhora significativa na memória espacial e no reconhecimento de objetos, além de reduzir a carga de placas Aβ no hipocampo e no córtex. Esses achados reforçam a hipótese de que a homeostase intestinal é um pré-requisito para a saúde neurológica e que a manipulação terapêutica do microbioma oferece uma janela de oportunidade sem precedentes para mitigar a neuroinflamação associada à PUFA.
Em suma, a compreensão de que a microbiota intestinal regula a patologia de Alzheimer através da sinalização de PUFAs e da ativação da via C/EBPβ/AEP redefine nossa abordagem terapêutica. A transição de um modelo de tratamento puramente paliativo para intervenções que visam o eixo microbiota-intestino-cérebro representa um avanço científico rigoroso. A modulação de metabólitos microbianos específicos e a restauração da eubiose surgem como estratégias assertivas para interromper a cascata neurodegenerativa, oferecendo esperança para o manejo de uma das doenças mais desafiadoras da medicina contemporânea.
Referência (ABNT): CHEN, Chun et al. Gut microbiota regulate Alzheimer’s disease pathologies and cognitive disorders via PUFA-associated neuroinflammation. Gut, [s. l.], v. 71, n. 11, p. 2233-2252, nov. 2022. Disponível em: https://doi.org/10.1136/gutjnl-2021-326269. Acesso em: 9 mai. 2026.