Estudos recentes sugerem que o Transtorno do Déficit de Atenção e Hiperatividade (TDAH) pode estar associado a maior risco de declínio cognitivo e de demência na vida adulta, incluindo a Doença de Alzheimer. Entretanto, essa associação deve ser interpretada com cautela: trata-se, mais provavelmente, de uma convergência de vulnerabilidades neurobiológicas, e não de uma relação causal linear. Em termos clínicos e neuroanatômicos, o TDAH pode refletir uma organização cerebral com menor eficiência em circuitos executivos, os quais também são frequentemente comprometidos ao longo da evolução do Alzheimer.
Do ponto de vista funcional, o elo entre as duas condições envolve principalmente as redes frontoparietais, frontoestriatais e frontocingulares, responsáveis por atenção sustentada, controle inibitório, memória de trabalho, planejamento, monitoramento de erros e flexibilidade cognitiva. No TDAH, essas redes já apresentam alteração desde o neurodesenvolvimento; no Alzheimer, elas sofrem comprometimento progressivo por neurodegeneração. Essa sobreposição ajuda a explicar por que indivíduos com TDAH podem, ao envelhecer, apresentar maior vulnerabilidade para declínio cognitivo.
Neuroanatomia envolvida
A relação entre TDAH e Alzheimer pode ser compreendida a partir de uma leitura por circuitos. No TDAH, as estruturas mais implicadas incluem o córtex pré-frontal dorsolateral, o córtex pré-frontal ventromedial, o córtex orbitofrontal, o cíngulo anterior, os gânglios da base, o tálamo e o cerebelo. Essas regiões participam da regulação da atenção, da inibição comportamental e da organização temporal da ação.
No Alzheimer, embora o início clássico envolva o lobo temporal medial, especialmente hipocampo e córtex entorrinal, a progressão da doença alcança redes associativas frontais e parietais, comprometendo memória episódica, linguagem, orientação, julgamento e funções executivas. Assim, o cérebro que já apresentava fragilidade nos circuitos de controle executivo por TDAH pode tornar-se mais suscetível ao impacto de processos degenerativos que atingem exatamente as mesmas redes.
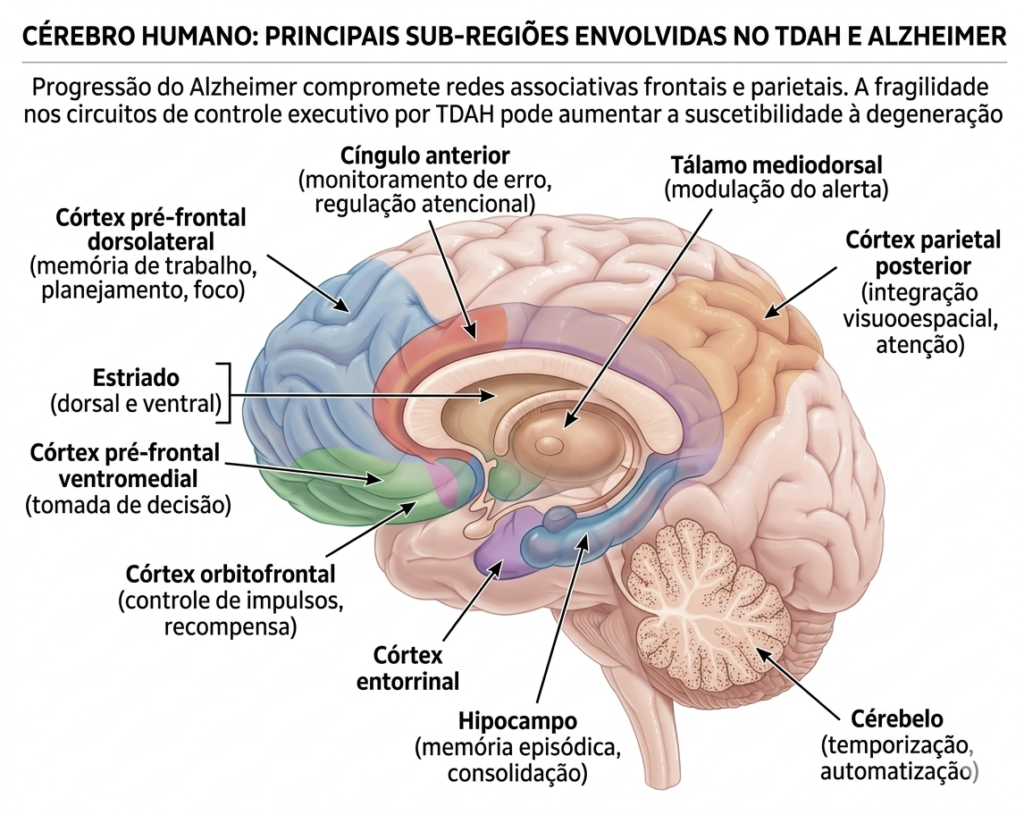
As principais subregiões podem ser organizadas assim:
– Córtex pré-frontal dorsolateral: memória de trabalho, planejamento e manutenção do foco.
– Córtex pré-frontal ventromedial e orbitofrontal: tomada de decisão, controle de impulsos e avaliação de recompensa.
– Cíngulo anterior: monitoramento de erro, esforço cognitivo e regulação atencional.
– Estriado dorsal e ventral: iniciação de resposta, hábito, motivação e processamento de recompensa.
– Tálamo mediodorsal: integração de informação e modulação do estado de alerta.
– Hipocampo e córtex entorrinal: memória episódica e consolidação mnésica.
– Córtex parietal posterior: integração visuoespacial e atenção dirigida.
– Cérebelo: temporização, automatização e modulação cognitiva.
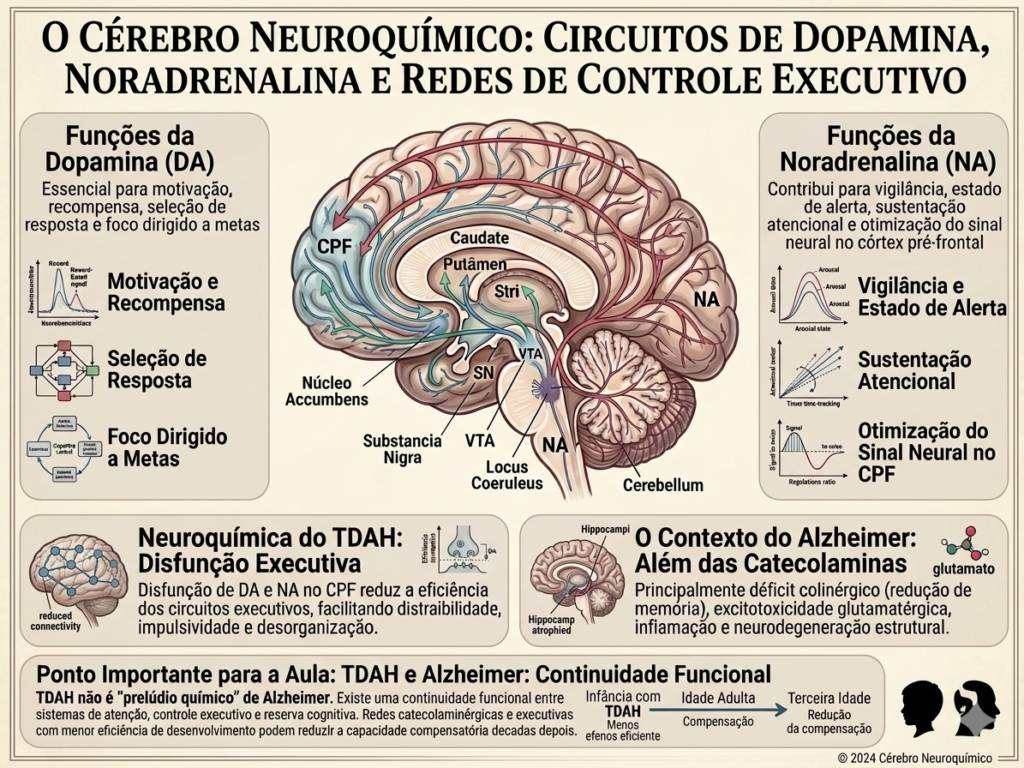
Neurotransmissores centrais
A base neuroquímica do TDAH envolve sobretudo dopamina e noradrenalina. A dopamina é essencial para motivação, recompensa, seleção de resposta e foco dirigido a metas; a noradrenalina contribui para vigilância, estado de alerta, sustentação atencional e otimização do sinal neural no córtex pré-frontal. A disfunção desses sistemas reduz a eficiência dos circuitos executivos e facilita distraibilidade, impulsividade e desorganização.
No Alzheimer, há participação importante da acetilcolina, cuja redução está relacionada a prejuízo de memória, atenção e aprendizagem. Além disso, a doença envolve alterações glutamatérgicas, inflamatórias e metabólicas, com disfunção sináptica progressiva. Portanto, enquanto o TDAH é mais fortemente associado a catecolaminas, o Alzheimer combina déficit colinérgico, excitotoxicidade e neurodegeneração estrutural.
Esse ponto é importante para a aula: o TDAH não é um “prelúdio químico” de Alzheimer, mas existe uma continuidade funcional entre sistemas de atenção, controle executivo e reserva cognitiva. Em outras palavras, quando redes catecolaminérgicas e executivas se desenvolvem com menor eficiência, a capacidade compensatória do cérebro pode ser menor décadas depois.
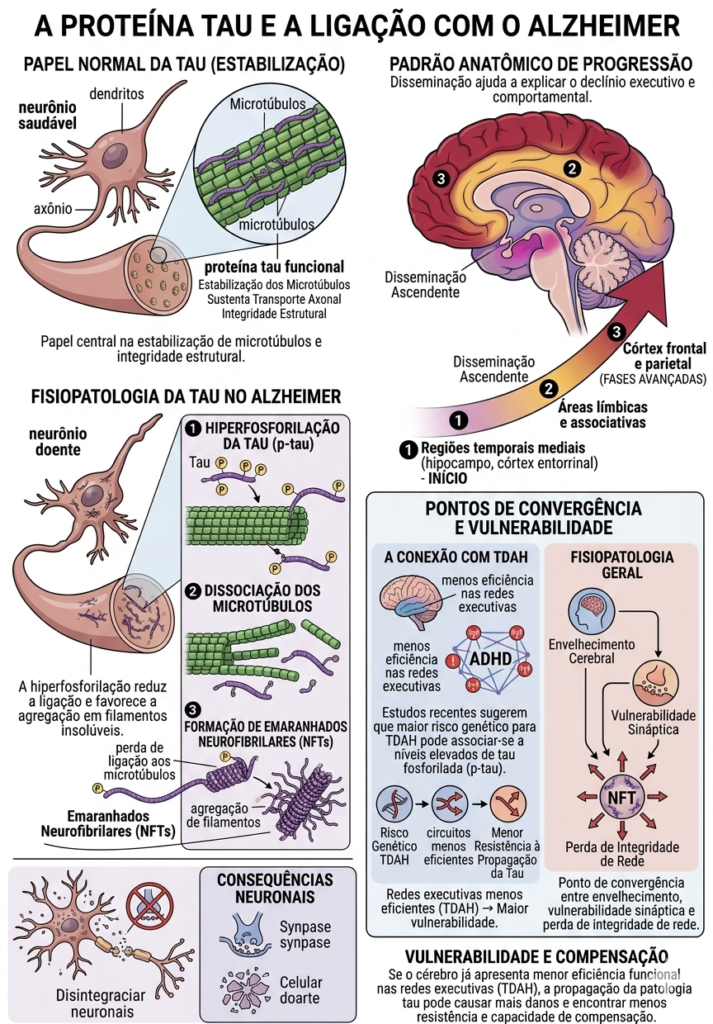
A proteína tau e a ligação com o Alzheimer
A proteína tau tem papel central na estabilização dos microtúbulos neuronais, sustentando o transporte axonal e a integridade estrutural do neurônio. No Alzheimer, ocorre hiperfosforilação da tau, o que reduz sua ligação aos microtúbulos e favorece agregação, formação de filamentos insolúveis e emaranhados neurofibrilares. Esses emaranhados estão associados a disfunção neuronal, perda sináptica e morte celular.
A progressão da patologia tau segue, em termos gerais, um padrão anatômico ascendente: inicialmente envolve regiões temporais mediais, depois se expande para áreas límbicas, associativas e, em fases mais avançadas, para córtex frontal e parietal. Essa disseminação ajuda a explicar o declínio executivo e comportamental na doença. Estudos recentes também sugerem que maior risco genético para TDAH pode associar-se a níveis elevados de tau fosforilada, sobretudo em indivíduos com biomarcadores de doença de Alzheimer, o que reforça a hipótese de sobreposição biológica entre neurodesenvolvimento e neurodegeneração.
Em termos fisiopatológicos, a tau pode ser entendida como um ponto de convergência entre envelhecimento cerebral, vulnerabilidade sináptica e perda de integridade de rede. Se o cérebro já apresenta menor eficiência funcional nas redes executivas, como ocorre no TDAH, a propagação da patologia tau pode encontrar menos resistência funcional e menos capacidade de compensação.
Como entender a ponte entre as duas doenças
A forma mais didática de explicar a relação é esta: o TDAH pode representar uma vulnerabilidade estrutural e funcional em redes de controle cognitivo; o Alzheimer, por sua vez, adiciona neurodegeneração progressiva sobre essas mesmas redes. Assim, o TDAH não “causa” Alzheimer, mas pode marcar um cérebro que envelhece com menor reserva funcional.
Essa ponte pode ser descrita em quatro etapas:
1. Alteração do neurodesenvolvimento em circuitos executivos.
2. Menor eficiência de modulação catecolaminérgica, especialmente dopaminérgica e noradrenérgica.
3. Menor reserva cognitiva e menor capacidade compensatória ao longo da vida.
4. Maior vulnerabilidade a processos neurodegenerativos, incluindo hipometabolismo, perda sináptica e patologia tau.
Esse modelo também ajuda a integrar fatores clínicos associados, como sono inadequado, depressão, sedentarismo, hipertensão, obesidade e estresse crônico, que podem agravar o risco de declínio cognitivo. Em pacientes com TDAH, esses fatores funcionam como amplificadores de vulnerabilidade.


